かんとこうブログ
2020.07.29
海水はなぜ錆びやすいのか?
今年の海の日は例外的に7月23日でした。今日は、海の日に因んで用意していたのですが、休日になったためブログに掲載できなかった話を書くことにします。
金属を海水に漬けるのと真水に漬けるのとで、どちらが錆びやすいでしょうか?と聞けば、誰もが海水と答えると思います。ではなぜ?と聞くと正しく答えられる人は少ないのではないでしょうか?金属を腐食から保護するというのは塗料のもつ最重要機能のひとつですので、塗料に働く人間としては知っておいて損はないと思います。少し難しい話も入りますが、説明したいと思います。
鉄を例にとって説明します。水の中で鉄が錆びるということは、鉄が溶けて鉄イオンになり、電子を放出することです。放出された電子は消費されないといけませんので、海水に溶けている酸素により水酸イオンが生成する際に消費されます。これを化学式で書くと(1)と(2)になります。学校で習っているはずですが、面倒ならばこんな式で表されるとだけ思ってくれれば結構です。肝心なことは式の内容ではなく、(1)の反応は簡単に起こりますが、(2)の反応は起こりにくいということであり、このため全体の反応がどのくらいの速さで進むのかは(2)の反応の速度が決めるということです。つまり海水中にとけている酸素(溶存酸素)の量が大切だということを理解してもらえば結構です。
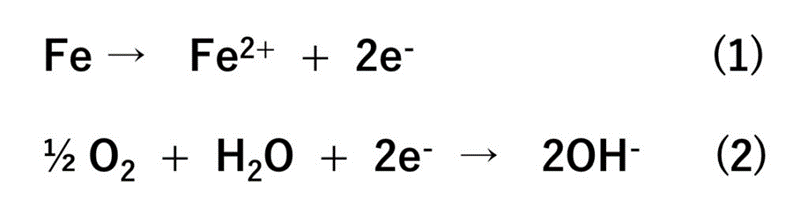
ただし、錆びる速さを決めるのは、溶存酸素の量だけではありません。海水中の電気の伝わり方(伝導度)が速くなければなりません。なぜなら電気が伝わらなければ、鉄表面が反応生成物でいっぱいになってしまい反応が停止してしまうからです。
ここで海水と真水の違いについて考えてみましょう。海水には食塩(塩化ナトリウム)をはじめ様々な塩(えん)が含まれており、その濃度は約3%程度です。pHも8付近であり、わずかにアルカリ側に偏っています。真水は塩濃度はゼロですが、空気中に放置すると炭酸ガスを吸収してわずかに酸性側に偏ります。pHだけみれば、真水の方が錆びやすそうに思えますがそうではありません。電導度が高いために(2)の反応が迅速に起こり、反応全体がが速くなるのです。
では塩分がもっと濃くなると錆びる速さはどうなるのでしょうか?実は海水の場合、3%程度の塩濃度が最も速く錆びることが知られています。これは、塩濃度が濃くなるにつれ電導度は確かに高くなるのですが、逆に溶存酸素が少なくなるからです。錆びるには3%付近が最もバランスがとれているということなのです。
それでは温度を上げていくとどうなるのでしょうか?温度を上げていくと80℃付近まではより早く錆びるようになりますが、それよりも温度が高くなると溶存酸素が減少するため錆びる速さは遅くなります。このように水中での鉄の錆びる速さは溶存酸素と電導度で決まるのです。
それでは海水中ではなく、空気中ではどうなのでしょうか?よく海岸の近くでは錆びやすいと言われます。事実海岸線から200メートル以内の建物は特別な配慮をしないとすぐに錆に覆われてしまいます。これは飛来する海塩粒子のせいです。
海塩粒子には塩化ナトリウムの他に、塩化マグネシウムなどの潮解性の塩も含まれています。一度錆が形成されると、この潮解性の塩が腐食をどんどん促進するのです。その様子を下図に示します。
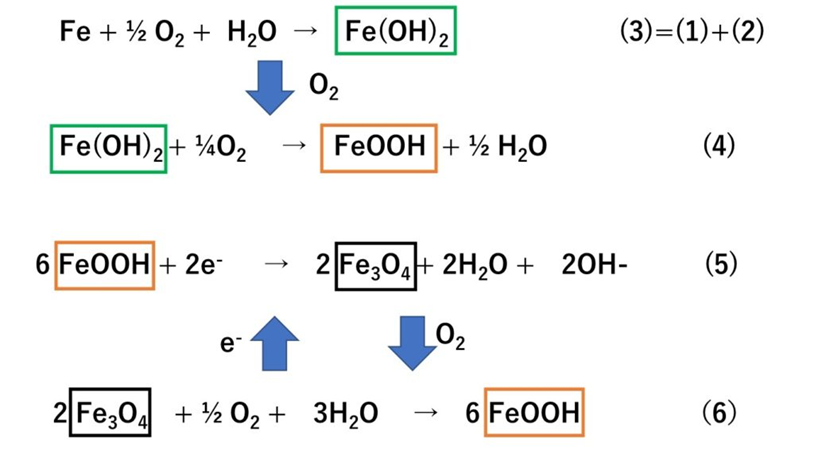
少し難しくなりますが詳しく説明します。(3)の式は、さきほどでてきた(1)と(2)を合わせて書いたもので、水中での鉄の錆を表わしています。生成するFe(OH)2は通常水に溶解しています。これがさらに酸化される(4)とFeOOHが生成し沈殿し、固形の錆ができます。
大気環境下では結露や降雨によって錆が生じます。金属表面に海塩粒子が存在していると、たとえ大気が低湿度であっても海塩粒子の潮解性のために金属表面は濡れた状態となります。(4)で生成するFeOOHは、海塩粒子存在下では、安定な結晶構造が作れず、金属表面に対し保護機能をもちません。
さらに重要なことは、このFeOOHは、水分が存在していると(5)により電子を消費し、Fe3O4を生成します。このことは、(1)で生成する電子をこの反応で消費できることを意味し、実際に鉄の溶解反応を進めます。さらにFe3O4も(6)によりまたFeOOHに戻ります。つまり、錆の中に水分が存在していると酸素の供給がなくともFeOOHが酸素の貯蔵庫となり、これらの腐食反応が継続的に進行するのです。
こうした鉄腐食のモデルを提唱者に因みエバンスサイクルと呼ばれています。詳しいメカニズムはともかく、海塩粒子が表面に存在することで生成した錆の内部に水分が存在し、この水分により腐食反応が継続する・・これが、海塩粒子が付着しやすい海浜地区で、腐食が極めて速く進行する理由です。
海水の中、あるいは海岸に近い海浜地区での鉄の腐食が速く進行する理由について説明しました。もし今度誰かに尋ねられたら、是非説明してあげてもらえればと思います。
今日書いた内容は、以下の資料(大阪府立大学大学院研究科 講師 井上 博之 「海水・塩水・さび -塩分があると金属はどうしてさびやすのか?-」 の内容を参考にしました。